(상하이 2023년 5월 29일 PRNewswire=연합뉴스) 중요한 미충족 의료 수요를 해결하는 치료제 개발에 전념하는 회사인 Altamira Therapeutics Ltd.(나스닥: CYTO)가 계절성 알레르기 비염(Seasonal Allergic Rhinitis, SAR) 환자를 대상으로 Bentrio 비강 스프레이를 평가하는 무작위 대조 NASAR 임상시험에서 긍정적이고 통계적으로 유의미한 톱라인 결과를 발표했다. Bentrio 비강 스프레이는 꽃가루나 집먼지진드기와 같은 공기 중 알레르겐으로부터 보호하기 위한 무약물 무방부제의 젤 에멀전으로 제조됐다.
NASAR 임상시험은 호주에서 100명의 SAR 환자를 등록했으며, 이들은 1:1 비율로 무작위 배정돼 Bentrio 또는 식염수 비강 스프레이를 2주 동안 하루 3회 또는 필요에 따라 자가 투여했다. 적격성을 위해, 환자는 지난 24시간 이내에 1주간의 무치료 런인 기간(Run-in Period)에 최악의 코막힘, 재채기, 비강 가려움증, 비루(콧물)의 최악 수준을 참조해 평균적으로 12점 중 최소 5점의 베이스라인 반사 총 비강 증상 점수(reflective Total Nasal Symptom Score, rTNSS)를 가져야 했다. 1차 유효성 평가변수는 후속 2주간의 치료 기간에 Bentrio와 무약물 SAR 관리의 현재 치료 표준인 식염수 비강 스프레이 사이의 평균 rTNSS의 차이로 정의됐다. 2주 동안 평균 rTNSS의 변화는 일반적으로 SAR 임상시험의 1차 유효성 평가변수로 인정되며, 이는 FDA에서도 권장하는 방식이다.
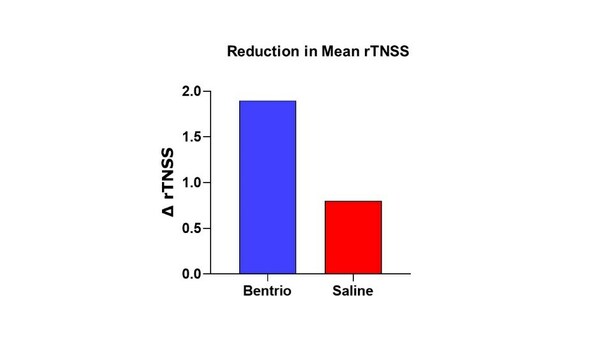
Graph above compares reduction in mean reflective Total Nasal Symptom Score (rTNSS) with Bentrio vs. saline nasal spray control over two weeks of treatment from baseline
14일의 치료 기간에, Bentrio 그룹에서 rTNSS는 치료 이전 기간의 6.9점에서 평균 5.0점으로 감소(-1.9점)한 반면, 식염수 스프레이 그룹은 6.9점에서 6.2점으로 감소(-0.8점)했다('평균 rTNSS' 그래프 참조). 따라서 Bentrio로 인한 비강 증상의 감소는 식염수 비강 스프레이를 사용했을 때보다 2.5배 더 큰 것으로 나타났다. Bentrio이 식염수 비강 스프레이 대비 rTNSS에서의 1.1점 감소 차이는 ANCOVA 모델에서 통계적으로 유의했으며(LSmeans; p = 0.012; 95% 신뢰 구간 -2.0 ~ -0.3), 따라서 이 연구는 1차 유효성 평가변수를 충족한 것으로 나타났다.
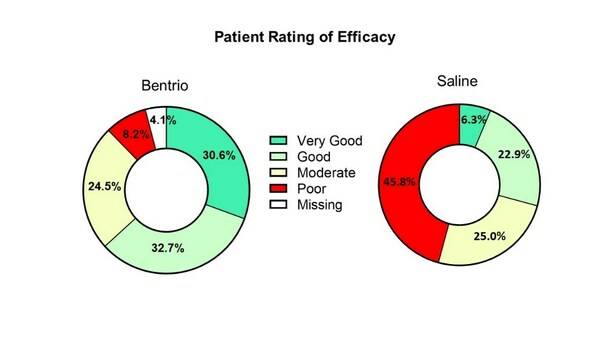
Graph above compares patient rating of treatment efficacy with Bentrio vs. saline nasal spray control after two weeks of treatment
Bentrio에서 나타난 치료 효과는 임상적으로 중요한 최소 차이인 0.28점을 훨씬 초과했다. Bentrio로 치료받은 연구 참가자의 63.3%가 치료 효과가 양호하거나 매우 양호하다고 평가한 반면, 식염수로 치료받은 참가자의 29.2%만이 치료 효과가 양호 또는 매우 양호하다고 답했다('환자 등급' 그래프 참조). 식염수로 치료받은 참가자 중 45.8%는 효능이 좋지 않다고 보고한 반면, Bentrio로 치료받은 그룹은 8.2%만이 효능이 좋지 않다고 평가했다. 식염수 치료 참가자의 85.5%가 치료 내약성을 양호 또는 매우 양호로 평가했으며, Bentrio 치료 참가자 중 그렇게 답한 참가자는 73.5%였다. 식염수 치료를 받은 참가자 중 10.4%는 내약성이 좋지 않다고 보고한 반면, Bentrio 그룹에서는 6.1%만이 내약성이 좋지 않다고 평가했다.
Altamira Therapeutics의 창립자이자 회장 겸 CEO인 Thomas Meyer는 "우리는 호주의 알레르기 계절 동안 실제 조건에서 얻은 NASAR 임상시험의 강력한 결과에 흥분을 감출 수 없다"며 "비강 증상의 큰 감소는 무약물 치료로 계절성 알레르기 비염에 대한 효과적인 보호가 이뤄질 수 있다는 것을 보여주는 것"이라고 말했다. 그는 "이는 약물 비강 스프레이에 효과가 없거나 방부제 또는 기타 성분의 내약성 문제로 인해 잘 반응하지 않는 많은 환자에게 도움이 될 것"이라면서 "이 중요한 임상 이정표에 도달할 수 있도록 도와준 NASAR 임상시험에 참여한 모든 환자와 연구자에게 진심으로 감사를 전한다"고 말했다.
또한, Meyer 대표는 "NASAR 결과는 Bentrio가 현재 표준 치료인 식염수 비강 스프레이 치료에 비해 통계적으로 유의하고 임상적으로 관련성이 높은 효능 개선이 있다는 것을 보여주는 것"이라며 "식염수 비강 스프레이의 경우 알레르겐 입자를 씻어내는 것을 목표로 하는 반면, Bentrio는 얇은 보호막을 형성해 이러한 입자가 비강 점막과 접촉하는 것을 방지하고 자연적인 점액 섬모 청소를 통해 알레르겐 입자를 제거하는 데 도움을 준다"고 설명했다. 이어 "이전 임상시험에서 이미 입증된 바와 같이, Bentrio는 비강 내에서 약 3.5시간 동안 머무르며 보호 효과를 발휘하는 반면, 식염수 스프레이는 약 1시간 동안만 비강 내에 존재하며 비강 내에서 더 좁은 분포와 더 적은 적용 범위를 제공한다"고 말했다.
한편, Meyer 대표는 "NASAR 임상시험이 완료됨에 따라, Altamira는 알레르기 비염 관리에 대한 Bentrio의 임상 개발을 마쳤다"라며 "2023년 처방전 없이 구매할 수 있는 알레르기 치료제의 미국 매출액은 약 40억 달러 규모로 추정되는데, 이는 비약물, 무방부제 치료 범주에서의 주요 기회를 잘 보여주는 것"이라고 말했다. 그러면서 "Altamira는 마케팅 및 유통 파트너와의 협력을 통해 환자가 알레르기 비염과 관련된 일상적인 부담과 불편함에 대처할 수 있는 효과적이고 안전한 치료 옵션으로 Bentrio를 제공할 수 있기를 기대하고 있다"고 부연했다.
Nuance Pharma의 CEO 겸 공동 설립자인 Mark G. Lotter는 "파트너인 Altamira Therapeutics가 Bentrio 임상 연구에서 이 중요한 이정표를 달성한 것을 매우 기쁘게 생각한다"며 "이 긍정적인 톱라인 결과를 바탕으로, 알레르기 비염 환자를 위한 새로운 무약물 및 무방부제 치료에 대한 전 세계적인 시급한 요구를 해결할 수 있는 Bentrio의 잠재력에 대해서도 매우 기쁘게 생각한다"고 말했다. 이어 "Altamira와 성공적이고 강력한 파트너십을 맺고, APAC 지역의 더 많은 국가에서 충족되지 않은 높은 의료 수요를 충족하기 위해 이 혁신적인 치료법을 제공하기를 기대한다"고 덧붙였다.
2022년 3월, Nuance Pharma와 Altamira Therapeutics는 중국 본토, 홍콩, 마카오 및 한국에서 Bentrio에 대한 독점 라이선스 및 유통 계약을 체결했다. 2022년 11월, Nuance Pharma는 중국의 홍콩에서 Bentrio 비강 스프레이를 출시한다고 발표했다.
Bentrio 소개
Bentrio는 공기 중 알레르겐 및 공기 중 바이러스(승인된 경우)로부터 개인을 보호하기 위한 OTC 무약물 비강 스프레이다. Bentrio를 코에 바르면 즉시 코점막에 보호 젤 층이 형성된다. 이 얇은 막은 알레르겐(또는 바이러스 입자)이 세포와 접촉하는 것을 방지하도록 고안됐다. 또한, 그 조성물은 이러한 입자를 결합시키고, 이들의 배출을 돕는 역할을 한다. 이는 알레르기 증상의 완화를 촉진(또는 상기도 바이러스 감염 완화)하도록 고안됐다. 더 자세한 내용은 웹사이트 https://www.aurismedical.com/legacy-programs/bentrio에서 확인할 수 있다.
Altamira Therapeutics소개
Altamira Therapeutics(나스닥: CYTO)는 간외 표적을 위한 RNA 전달 기술(OligoPhore(TM) / SemaPhore(TM) 플랫폼)을 개발 및 상업화하는 데 전념한다. 회사는 현재 생체 내 개념 증명을 넘어 전임상 개발 단계에 있는 2건의 대표적인 siRNA 프로그램인 암을 유발하는 KRAS용 AM-401과 류머티즘 관절염용 AM-411를 보유하고 있다. 이 다기능 전달 플랫폼은 mRNA 및 기타 유형의 RNA 치료제에도 적합하며, 제약 또는 생명 공학 회사에 대한 아웃 라이선스를 통해 활용될 계획이다. 또한, Altamira는 알레르기 및 바이러스 감염(Bentrio(R) OTC 비강 분무기, 상업용)과 내이 치료제(현기증에 대한 AM-125 비강 분무기, 2상 후, 이명 및 청력 손실에 대한 Keyzilen(R) 및 Sonsuvi(R), 3상)에 대한 기존 자산을 매각 또는 아웃 라이선스하는 과정에 있다. 2003년에 설립된 Altamira는 버뮤다 해밀턴에 본사를 두고 있으며, 스위스 바젤에서 주요 사업을 운영하고 있다. 더 자세한 내용은 웹사이트 https://altamiratherapeutics.com/에서 확인할 수 있다.
Nuance Pharma 소개
Nuance Pharma는 후기 단계 임상 파이프라인과 상업 단계 자산 포트폴리오를 모두 갖춘 혁신 중심의 바이오 제약 회사다. 전문적인 치료에 중점을 둔 Nuance는 호흡기, 통증 관리, 응급 치료 및 철 결핍성 빈혈 전반에 걸친 상업화된 자산과 혁신적인 파이프라인의 차별화된 조합을 구축했다.
Nuance는 아시아태평양 지역의 중요한 미충족 의료 수요를 해결한다는 사명에 따라 세계 선도적인 혁신적인 파이프라인을 개발하는 듀얼 휠(Dual Wheel) 모델을 구축하는 한편, 중국과 아시아 지역 모두에서 자체적으로 지속가능한 상업적 운영을 유지하고 있다. 더 자세한 내용은 웹사이트 www.nuancepharma.com에서 확인할 수 있다.
전향적 진술
본 보도자료에는 위험, 불확실성 및 기타 요소가 포함된 전향적 진술이 포함된다. 그중 다수는 회사의 통제 범위 밖에 있으며, 실제 결과는 본 전향적 진술에서 논의된 결과와 상당히 다를 수 있다. 전향적 진술에는 회사의 계획, 목표, 미래 사건, 성과 또는 과거 정보가 아닌 기타 정보에 관한 진술도 포함된다. 모든 전향적 진술은 이러한 경고성 진술 및 전향적 진술에 수반될 수 있는 기타 경고성 진술에 의해 명시적으로 제한이 부여된다. 회사는 법률에서 요구하는 경우를 제외하고 해당 날짜 이후에 발생된 사건이나 상황을 반영하기 위해 전향적 진술을 공개적으로 갱신하거나 수정할 의무가 없다.